Khi làm quen với bộ môn hóa học, chắc hẳn bạn đã từng nghe đến khái niệm phân tử. Vậy phân tử là gì? Có mấy loại phân tử? Sự khác biệt giữa phân tử và nguyên tử là gì? Cùng tìm câu trả lời trong nội dung bài viết dưới đây của supperclean.vn
Contents
Phân tử là gì?
Chương trình Hóa Học lớp 8 đã giải thích phân tử là gì như sau: Phân tử là hạt đại diện và thể hiện tính chất hóa học của chất, do một hoặc nhiều nguyên tử kết hợp với nhau bằng liên kết hóa học.
Ví dụ về phân tử:
- Phân tử đường glucose C6H12O6 gồm 6 nguyên tử C, 12 nguyên tử H và 6 nguyên tử O liên kết với nhau.
- Phân tử rượu etylic C2H6O gồm có 2 nguyên tử C, 6 nguyên tử H và 1 nguyên tử O liên kết với nhau.

Có mấy loại phân tử?
Phân tử được chia thành 2 loại, đó là:
Phân tử của đơn chất
Phân tử của đơn chất là phân tử được hình thành từ các nguyên tử cùng loại liên kết với nhau.
Ví dụ về phân tử đơn chất:
- Phân từ khí oxi gồm 2 nguyên tử oxi liên kết tạo thành.
- Phân tử khí hidro gồm 2 nguyên tử hidro liên kết với nhau tạo thành.
- Phân tử khí nitơ được tạo thành bởi 2 nguyên tử nitơ,..
Phân tử của hợp chất
Phân tử của hợp chất được tạo thành do các nguyên tử khác loại liên kết với nhau.
Ví dụ về phân tử của hợp chất:
- Phân tử nước gồm có 2 nguyên tử H và 1 nguyên tử O liên kết với nhau.
- Phân tử muối ăn gồm 1 nguyên tử Na liên kết với 1 nguyên tử Cl
- Phân tử carbon dioxide được hình thành từ 2 nguyên tử O liên kết với 1 nguyên tử C
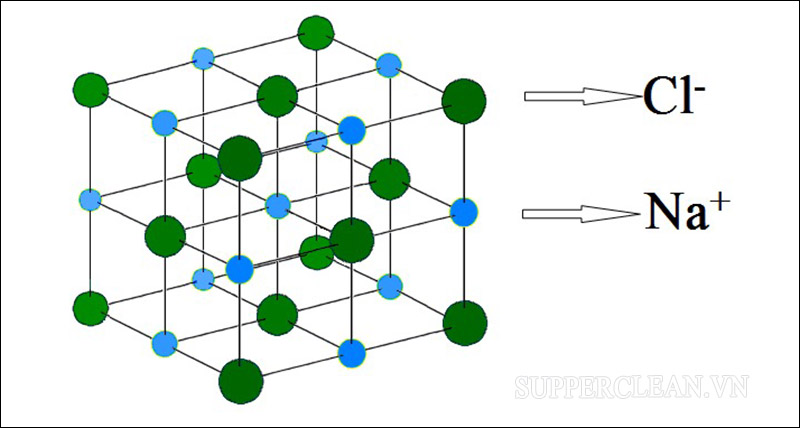
Quá trình hình thành phân tử hóa học là gì?
Các nguyên tử chỉ gồm có 1 hạt nhân duy nhất mang điện tích dương và bảo quanh nó là các electron mang điện tích âm. Khi các nguyên tử tiếp cận nhau trong phạm vi gần, các electron sẽ phản ứng với nhau và phản ứng với hạt nhân. Tương tác này khiến cho tổng năng lượng của hệ giảm xuống và các nguyên tử sẽ liên kết với nhau tạo thành phân tử.
Như vậy, phân tử được hình thành từ các nguyên tử thông qua liên kết hóa trị.

Liên kết phân tử là gì?
Liên kết phân tử là các liên kết cộng hóa trị. Các nguyên tử có thể liên kết với nhau theo một tỷ lệ nhất định để hình thành phân tử. Điều này tạo nên sự khác biệt của các hợp chất hóa học khác nhau.
Ví dụ, hidro và oxi có thể xuất hiện trong bất kỳ hỗn hợp cơ học nào nhưng khi nhắc đến nước thì chúng chỉ kết hợp với nhau theo tỷ lệ 2H:1O. Nếu thay đổi tỷ thì sẽ hình thành phần tử khác. Ví dụ 2 nguyên tử H liên kết với 2 nguyên tử O sẽ tạo thành phân tử hydrogen peroxide (H2O2).
Ngoài ra, các nguyên tử có thể liên kết với nhau theo tỷ lệ như nhau nhưng khác vị trí liên kết để tạo ra các phân tử khác nhau. Các phân tử như vậy được gọi là đồng phân. Ví dụ như methyl ether và ethyl alcohol đều có 2 C, 6H và 1 O nhưng các nguyên tử này lại liên kết với nhau theo các cách khác nhau.
Khối lượng phân tử là gì?
Khối lượng phân tử là tổng khối lượng các nguyên tử hình thành nên phân tử. Đơn vị tính khối lượng phân tử là amu.
Để tính khối lượng phân tử, bạn thực hiện theo các bước sau:
- Bước 1: Dựa vào ký hiệu hóa học, hãy xác định nguyên tử khối của từng nguyên tử cấu tạo nên phân tử.
- Bước 2: Nhân nguyên tử khối với số khối tương ứng của nguyên tử trong phân tử.
- Bước 3: Cộng các tích vừa tính được ở bước 2 lại với nhau.
Ví dụ: Phân tử carbon dioxide (CO2) được cấu thành từ 1 C và 2 O. Khối lượng phân tử CO bằng 12 + 16 x 2 = 48 amu.

Sự khác biệt giữa phân tử và nguyên tử là gì?
| Đặc điểm so sánh | Phân tử | Nguyên tử |
| Bản chất | Phân tử là các hạt mang đầy đủ tính chất hóa học của chất. | Hạt có kích thước siêu nhỏ và trung hòa về điện. |
| Cấu tạo | Cấu tạo từ một số nguyên tử liên kết với nhau. | Gồm có hạt nhân nguyên tử (nơtron và proton) và vỏ nguyên tử (electron). |
| Hình dạng | Nhiều hình khác nhau. | Có dạng hình cầu. |
| Tính chất | Các nguyên tử trong phân tử có thể tách rời và kết hợp lại với nhau. | Không thể phân đôi nguyên tử được. |
| Sự tồn tại | Tồn tại được trong trạng thái tự do. | Có thể hoặc không thể tồn tại ở trạng thái tự do. |
| Khả năng quan sát | Không thể quan sát được bằng mắt thường nhưng có thể quan sát dưới kính hiển vi. | Không thể nhìn thấy được bằng mắt thường hay kính hiển vi. |
| Khả năng phản ứng | Ít phản ứng. | Cao. |
| Liên kết hình thành | Liên kết cộng hóa trị | Liên kết hạt nhân. |
Bài tập minh họa về phân tử
Bài tập 1: Mô hình phân tử nào của đơn chất?
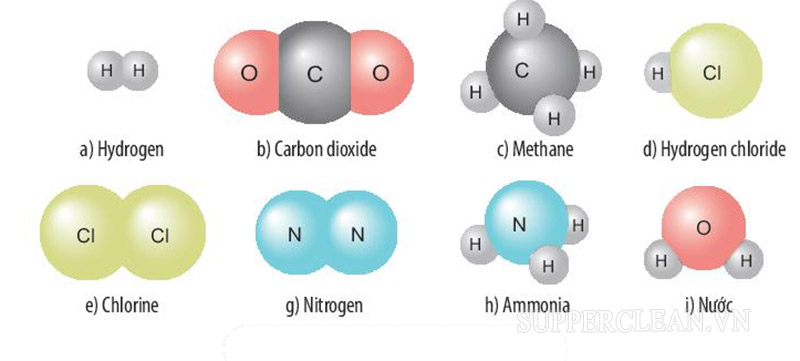
Lời giải:
Mô hình phân tử của đơn chất là: a, e, g
Mô hình phân tử của hợp chất: b, c, d, h, i
Bài tập 2: Phân tử A gồm có nguyên tố oxygen và carbon. Tính khối lượng phân tử A?
Lời giải:
Theo như đề bài, phân tử A có thể là CO2 hoặc CO.
- Nếu A là CO thì khối lượng phân tử bằng 12 + 16 = 28 amu
- Nếu A là CO2 thì khối lượng phân tử bằng 12 + 16 x 2 = 48 amu
Bài tập 3: Trong mật ong có chứa rất nhiều phân tử fructose. Trong đó, 1 phân tử fructose gồm có 6 nguyên tử C, 6 nguyên tử O và 12 nguyên tử H. Vậy fructose là loại phân tử nào? Hãy tính khối lượng nguyên tử của nó?
Lời giải:
Phân tử fructose là loại phân tử hợp chất bởi nó được tạo thành từ nhiều nguyên tố khác nhau.
Công thức phân tử của fructose là C6H12O6
=> Khối lượng phân tử của fructose là 12 x 6 + 1 x 12 + 16 x 6 = 180 amu
Bài tập 4: Từ ba nguyên tố là C, O, H, hãy liệt kê 5 phân tử mà em biết và tính khối lượng phân tử của chúng?
Lời giải:
Các phân tử được cấu thành từ các nguyên tử C, H, O là H2O (nước), CO (carbon monoxide), CO2 (carbon dioxide), O2 (oxygen), CH4 (methane).
- Khối lượng phân tử nước là 1 x 2 + 16 = 18 amu
- Khối lượng phân tử carbon monoxide là 12 + 16 = 28 amu
- Khối lượng phân tử carbon dioxide là 12 + 16 x 2 + 48 amu
- Khối lượng phân tử methane là 12 + 1 x 4 = 16 amu
XEM THÊM:
Trên đây là bài viết chia sẻ toàn bộ thông tin về phân tử là gì. Hy vọng sẽ mang đến nhiều kiến thức ôn luyện hữu ích cho bạn đọc! Supperclean.vn chúc các bạn luôn học tốt và đạt điểm cao nhé!




