Liên kết ion là liên kết thường gặp trong các liên kết hóa học giữa nguyên tử nguyên tố phi kim và nguyên tử nguyên tố kim loại. Vậy liên kết ion là gì? Có bản chất gì? Mời bạn đọc cùng supperclean.vn ôn luyện lại nhé!
Contents
Liên kết ion là gì? Bản chất của liên kết ion là gì?
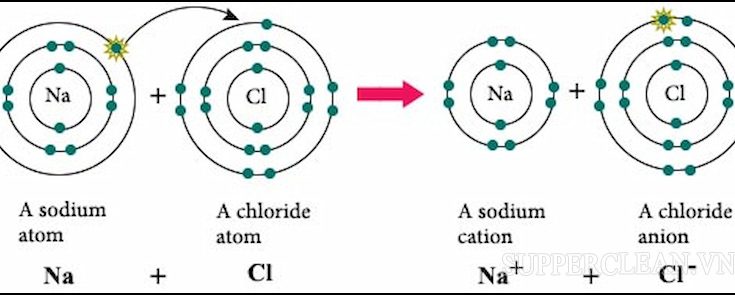
Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái ngược nhau. Liên kết này thường xảy ra giữa nguyên tử của nguyên tố phi kim với nguyên tử nguyên tố kim loại.
Ví dụ: Liên kết giữa cation Na+ với anion Cl- chính là liên kết ion.
Na(+) + Cl(-)→ NaCl
Bản chất liên kết ion là lực hút tĩnh điện giữa hai ion trái dấu nhau. Do vậy, liên kết ion còn được gọi là liên kết điện tích.
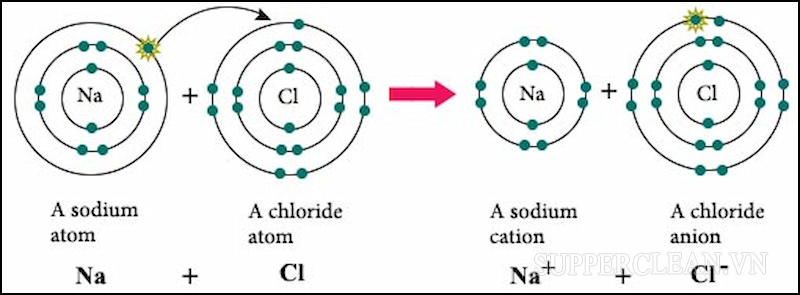
Trong phản ứng hóa học, khi các phân tử, nguyên tử thêm/ mất electron sẽ tạo thành phần tử mang điện tích, gọi là ion. Ion được chia thành 2 loại, đó là:
- Ion dương (cation): Khi tham gia phản ứng hóa học, nếu các nguyên tử nhường bớt electron thì nó sẽ trở thành phần tử mang điện tích dương.
- Ion âm (anion): Nếu các nguyên tử nhận thêm electron trong quá trình tham gia phản ứng hóa học sẽ trở thành phần tử mang điện tích âm.
Điều kiện hình thành sự liên kết ion là gì?
Liên kết ion được hình thành khi thỏa mãn 2 điều kiện sau:
- Được hình thành bởi các nguyên tố có tính chất hóa học khác nhau, ví dụ như giữa phi kim và kim loại điển hình.
- Sự chênh lệch về độ âm điện giữa 2 nguyên tử liên kết quy ước là ≥1.7, ngoại trừ một số trường hợp ngoại lệ.
Dấu hiệu nhận biết liên kết ion là gì?
Từ điều kiện hình thành, ta có một số dấu hiệu nhận biết liên kết ion như sau:
- Các phân tử của hợp chất được hình thành từ kim loại điển hình cho đến phi kim điển hình. Ví dụ như BaF2, CaCl2,… đều chứa liên kết ion bởi chúng được hình thành giữa cation kim loại và anion phi kim.
- Các phân tử của hợp chất muối có chứa cation hoặc anion đa nguyên tử. Ví dụ như Al2(SO4)3, AgNO3,… đều là liên kết ion, được hình thành giữa cation kim loại với anion gốc axit.
Liên kết ion có tính chất gì?
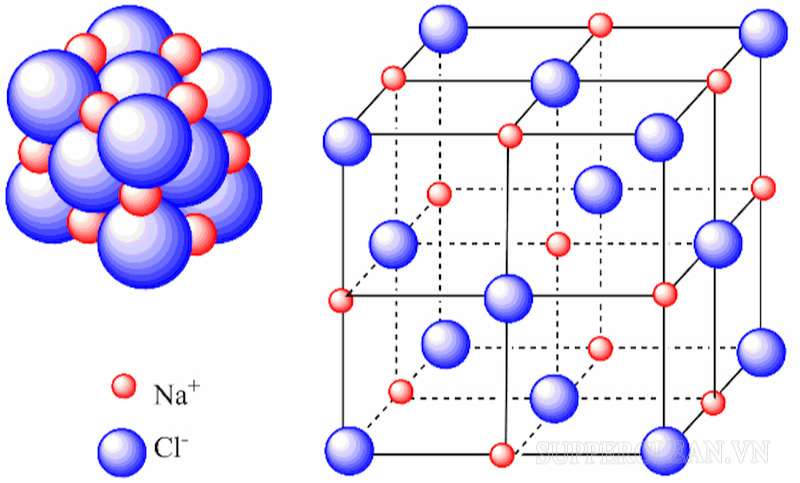
Liên kết ion là sự kết hợp của nhiều ion lại với nhau tạo thành phân tử khổng lồ. Sự sắp xếp của một cấu hình học như vậy gọi là mạng tinh thể ion.
Ví dụ, phân tử NaCl không chỉ chứa 1 ion Na và 1 ion Cl mà chúng chứa rất nhiều ion Na, Cl theo tỷ lệ 1:1.
Thông thường, các liên kết ion sẽ có tính chất sau:
- Ở trạng thái rắn, ion tồn tại trong nhiệt độ phòng và dưới dạng tinh thể.
- Các ion sẽ được sắp xếp theo cấu trúc mạng tinh thể.
- Ở thể rắn, ion thường không dẫn điện. Tuy nhiên, khi tồn tại dưới dạng dung dịch, ion có khả năng dẫn điện.
- Khi đặt dưới áp lực, các ion rất dễ vỡ, đồng thời liên kết bị phá vỡ dọc theo mặt phẳng.
- Liên kết kết ion có lực hút tĩnh điện mạnh và tương đối bền vững. Vì vậy, các hợp chất ion thường khá cứng, có nhiệt độ sôi và nhiệt độ nóng chảy cao.Ví dụ, NaCl nóng chảy ở nhiệt độ khoảng 800 độ C.
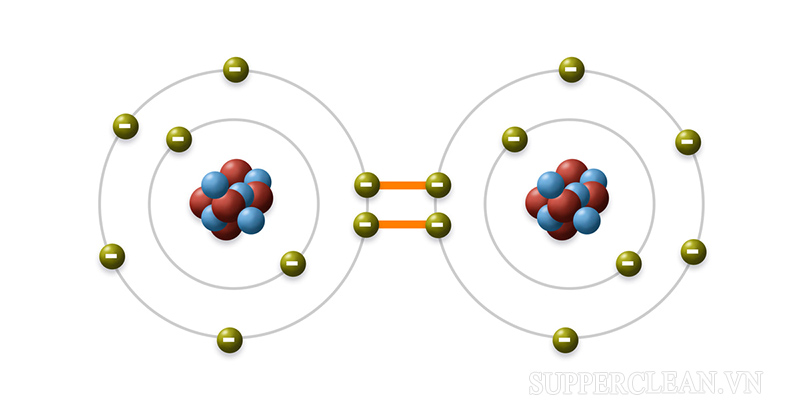
Điểm khác biệt giữa liên kết cộng hóa trị và liên kết ion là gì?
| Liên kết ion | Liên kết hóa trị | |
| Bản chất | Là lực hút tĩnh điện giữa các ion trái dấu nhau. | Liên kết giữa các nguyên tử dùng chung một hoặc nhiều cặp electron. |
| Hiệu độ âm điện | Hiệu độ âm điện ≥1.7 | 0 < Hiệu độ âm điện < 1.7 |
Bài tập về liên kết ion
Ví dụ 1: Phân tử nào dưới đây mang nhiều đặc điểm của liên kết điện tích nhất?
- NaCl
- CsCl
- LiCl
=> Chọn đáp án b.
Ví dụ 2: Dãy nào dưới đây đều chứa liên kết ion?
- K2O, MgO, KBr
- CO2, CH4, HBr
- KBr, MgS, CS2
=> Chọn đáp án a.
Ví dụ 3: Hai ion Na+ và Cl- có cấu hình electron giống loại khí hiếm nào?
Lời giải:
Ion Na+ có 10 electron ở lớp vỏ, 8 electron ở lớp ngoài cùng và có 2 lớp electron => Có cấu hình giống với khí Ne: 1s22s22p6
Ion Cl-1 có 3 lớp electron và 18 electron tại lớp ngoài cùng => Có cấu hình giống với Ar: 1s22s22p63s23p6
Ví dụ 4: Ion Na+ rất quan trọng đối với cơ thể con người nhưng nếu dùng quá liều lượng sẽ dẫn đến các vấn đề về thận, tim mạch. Các nhà khoa học khuyến cáo lượng Na+ nạp vào cơ thể mỗi ngày không quá 2300mg và không ít hơn 500mg. Nếu một người ăn 5g muối mỗi ngày thì có vượt mức giới hạn cho phép không?
Lời giải:
NaCl → Na+ + Cl–
58.5g → 23g
5g → ?(g)
Lượng Na+ mà người này nạp vào cơ thể mỗi ngày là 1,966g = 1966mg
Như vậy: 500 < 1966 < 2300
=> Khi nạp 5g muối ăn mỗi ngày thì lượng Na+ nạp vào cơ thể không vượt quá giới hạn cho phép.
XEM THÊM:
Trên đây là toàn bộ kiến thức chia sẻ liên kết ion là gì lớp 7. Mong rằng bài viết này sẽ giúp ích cho bạn đọc trong quá trình học tập. Đừng quên theo sõi Supperclean để cập nhật nhiều kiến thức thú vị hoen nhé.