Phản ứng thế là một phản ứng thường gặp trong hóa học. Vậy thì hãy supperclean.vn tìm hiểu phản ứng thế là gì và điểm qua một số dạng bài tập thường gặp trong bài viết này nhé!
Contents
Phản ứng thế là gì? Cho ví dụ minh họa
Theo như sách Hóa Học lớp 8 đã giải thích phản ứng thế là gì như sau:
“Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất”.
Ví dụ về phản ứng thế:
- Fe + 2HCl → FeCl2 + H2 => Trong phản ứng này, nguyên tử sắt (Fe) đã thế chỗ cho nguyên tử Clo trong hợp chất FeCl2.
- 3Mg + 2AlCl3 → 2Al + 3MgCl2 => Nguyên tử magie (Mg) đã thế chỗ cho nguyên tử nhôm (Al) trong hợp chất AlCl3.
Về bản chất, phản ứng thế là phản ứng hóa học xảy ra ở điều kiện cụ thể về áp suất và nhiệt độ, nguyên tố hóa học hoạt động mạnh hơn (trong đơn chất) sẽ đẩy nguyên tố hoạt động hóa học yếu hơn trong hợp chất và thay thế chúng.
Phản ứng thế là gì? – Phân loại
Trong hóa học, phản ứng thế được chia thành 2 loại, đó là:
Phản ứng thế trong hóa vô cơ
- Số oxi hóa của người tố bị thay đổi.
- Phương trình minh họa: A + BX → AX + B (ở điều kiện áp suất và nhiệt độ cụ thể, A có khả năng hoạt động hóa học mạnh hơn B).
Ví dụ minh họa:
- 2Al + 6HCl → 2AlCl3 + 3H2
- Fe + H2SO4 → H2 + FeSO4
- 3Cl2 + 2NH3 → 6HCl + N2
- Fe + CuCl2 → Cu + FeCl2
- Zn + CuCl2 → Cu + ZnCl2
- 2C + SiO2 → 2CO + Si
- 2HCl + Zn → H2 + ZnCl2
XEM THÊM: Quán tính là gì? Lực quán tính là gì? Ví dụ, công thức tính
Phản ứng thế trong hóa hữu cơ
Trong hóa học hữu cơ, phản ứng thế là phản ứng hóa học; trong đó một nhóm của hợp chất này được thay thế bằng nhóm khác. Có 3 loại phản ứng thế phổ biến của hợp chất hữu cơ, đó là:
- Thế ái lực hạt nhân
- Thế ái lực điện tử
- Thế gốc
Vì chúng là một dạng phản ứng dây chuyền nên cần phải có điều kiện ánh sáng hoặc bổ sung các chất dễ phân hủy thành gốc tự do (hoạt động) vào.
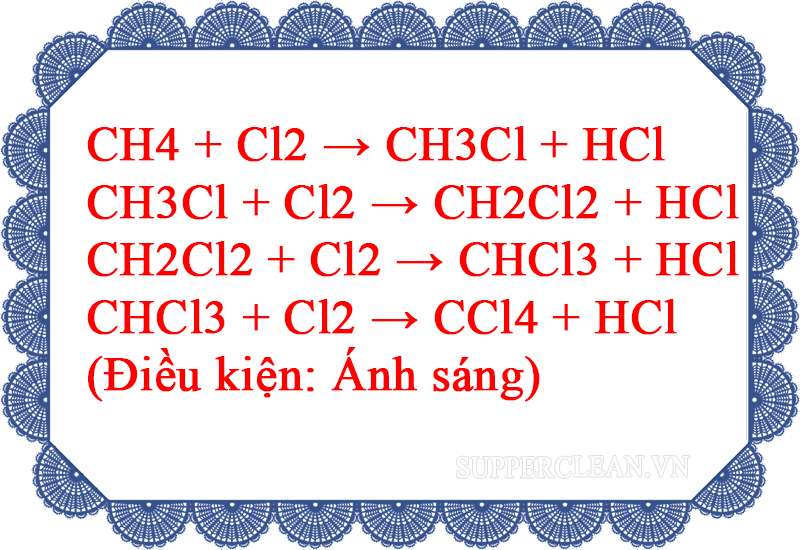
Ví dụ: Tham khảo quá trình phản ứng giữa Clo và Metan trong hình minh họa dưới đây:

Một số phản ứng hóa học khác
Ngoài phản ứng thế, trong hóa học còn có một số phản ứng khác như:
Phản ứng cộng
Đây là phản ứng mà trong đó các phân tử của hợp chất hữu cơ kết hợp với các phân tử khác, tạo thành hợp chất mới.
Ví dụ:
- C2H4 + Br2 → C2H4Br2
- C2H4 + HCl → C2H5Cl (điều kiện: nhiệt độ, HgCl2)
Phản ứng tách
Là phản ứng mà trong đó hai hoặc nhiều nguyên tử bị tách ra khỏi phân tử hợp chất hữu cơ.
Ví dụ: CH3 – CH2 – OH → CH2 = CH2 + H2O (điều kiện: nhiệt độ, H2SO4)
XEM THÊM: Etanol là gì? Tính chất hóa học và ứng dụng của Etanol
Các dạng bài tập về phản ứng thế và phương pháp giải
Phản ứng thế halogen của ankan
– Lưu ý chung:
- Trong điều kiện thường, ankan có đặc điểm là tương đối trơ về mặt hóa học.
- Ankan không bị oxi bởi những dung dịch sau đây: HNO3, H2SO4, KMnO4,…
- Khi có điều kiện là nhiệt độ, ánh sáng và các chất xúc tác, ankan có khả năng tham gia các phản ứng tách, thế và oxi hóa
- Khi xét phản ứng thế halogen, người ta thường xét chúng khi phản ứng với Br2 và Cl2. Số lượng H bị thế sẽ phụ thuộc vào tỷ lệ model của halogen và ankan. Nguyên tử H của C có bậc cao hơn sẽ dễ bị thay thế hơn nguyên tử H của C có bậc thấp hơn.
– Phương pháp giải:
- Bước 1: Viết phương trình hóa học phản ứng giữa ankan với Br2 hoặc Cl2. Nếu đề bài không cho biết tên sản phẩm thế là gì ta sẽ viết dưới dạng tổng quát như sau:
- Bước 2: Tính khối lượng mol sản phẩm thế hoặc khối lượng mol trung bình hỗn hợp sản phẩm để tìm số nguyên tử cacbon (của ankan) hoặc mối liên hệ giữa cacbon với nguyên tử brom hoặc clo có trong sản phẩm thay thế. Từ đó, xác định công thức cấu tạo ban đầu của ankan và công thức của sản phẩm thay thế.

Phản ứng thế Hidrocacbon
Phản ứng thế Hidrocacbon là quá trình trong đó một nhóm thế (tức là một phân tử hoặc một nguyên tử) được thay thế trên một phân tử hidrocacbon bởi một nhóm thế khác. Phản ứng này xảy ra khi một hidrocacbon tương tác với một chất tác nhân thế.
XEM THÊM: Dòng điện trong kim loại là gì? Bản chất và ứng dụng

Một số bài tập về phản ứng thế
Ví dụ 1: Đâu là phản ứng thế trong các ví dụ minh họa dưới đây:
- 3CO + Fe2O3 → 2Fe + 3CO2.
- Fe + CuCl2 → FeCl2 + Cu
- FeCl2 + Cu → 2KCl + 3O2↑
- CaO + CO2 → CaCO3
Lời giải:
Chọn đáp án: b
Ví dụ 2: Có bao nhiêu phản ứng thế trong các phản ứng hóa học sau:
- Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
- K2O + H2O → 2KOH
- Zn + H2SO4 → ZnSO4 + H2↑
- CuO + 2HCl → CuCl2 + H2O
- Mg + CuCl2 → MgCl2 + Cu
- HCl + NaOH → NaCl + H2O
Lời giải:
Chọn đáp án b, gồm có các phản ứng số 1, 3 và 5.
Ví dụ 3: Cho kẽm tác dụng với HCl dư. Khối lượng kẽm cần dùng là bao nhiêu để điều chế được 1.12 lít khí hidro trong điều kiện tiêu chuẩn?
Lời giải:
Ta có phương trình:
Zn + 2HCl → ZnCl2 + H2↑
Số mol khí hidro là: 1.12/ 22.4 = 0.05 mol
=> Số mol kẽm = 0.05 mol
=> Khối lượng kẽm cần dùng = 0.05 x 65 = 3.25g
Ví dụ 4: Cho m (g) kẽm tác dụng với Hcl dư. Lượng khí hidro thu được tác dụng vừa đủ với 12g đồng (II) oxit. Khối lượng của kẽm là bao nhiêu?
Lời giải:
Phương trình:
Zn + 2HCl → ZnCl2 + H2↑ (1)
CuO + H2 → Cu + H2O (2)
Số mol của đồng (II) oxit = 12/80 = 0.15 mol
Theo phương trình hóa học 2 thì số mol khí H2 bằng số mol CuO = 0.15 mol.
=> Số mol Zn = Số mol H2 (theo phương trình 1)
=> Khối lượng kẽm = 0.15 x 65 = 9.75g
Bài viết này của supperclean.vn đã giúp bạn đọc tổng hợp kiến thức về phản ứng thế là gì và các dạng bài tập liên quan. Nếu bạn có góp ý hay câu hỏi thắc mắc thì hãy để lại bình luận bên dưới cho mình biết nhé!